《柳叶刀》子刊 EBioMedicine发表第三代EGFR-TKI艾维替尼的耐药机制研究
发布时间:2019-05-05

文章题为:Analysis of resistance mechanisms to abivertinib, a third-generation EGFR tyrosine kinase inhibitor, in patients with EGFR T790M-positive non-small cell lung cancer from a phase I trial(《第三代EGFR-TKI艾维替尼在晚期EGFR T790M突变阳性非小细胞肺癌患者中的耐药机制探索》)
2019年4月24日,国际权威医学期刊《柳叶刀》(The Lancet)子刊EBioMedicine在线发表了由广东省肺癌研究所吴一龙教授、周清教授共同领导的艾维替尼耐药机制研究。
依托艾维替尼I期剂量递增/拓展临床研究(NCT02330367),该研究纳入于广东省肺癌研究所入组I期临床研究且在艾维替尼疾病进展时接受耐药样本二代测序的患者,揭示了艾维替尼耐药基因谱的异质性与药物特异性。
艾维替尼(Abivertinib, AC0010)是我国自主研发的首个第三代EGFR-TKI创新药物, 具有与第三代EGFR-TKIs奥希替尼、CO-1686和WZ4002不同的化学结构。在既往EGFR-TKIs治疗失败、EGFR T790M突变阳性晚期非小细胞肺癌患者中开展的I期临床研究(NCT02330367)中,艾维替尼显示了良好的疗效和安全性。
What we know from this study?
研究纳入截至2018年10月30日,30例于广东省肺癌研究所入组艾维替尼I期临床研究且在艾维替尼治疗疾病进展时接受样本二代测序的患者,以探索艾维替尼的耐药机制。27例 (90%)患者提供了艾维替尼耐药血浆样本(其中21例仅提供血浆样本,4例提供配对血浆/组织样本,2例提供配对血浆/脑脊液样本)进行二代测序;3例(10%) 患者仅提供耐药组织样本二代测序。
上述30例患者中的部分经知情同意,接受了艾维替尼治疗基线、每次疗效评价直至艾维替尼治疗失败的连续血浆样本的二代测序,用于研究预存性(艾维替尼治疗前即存在)与获得性(艾维替尼治疗后新出现)耐药机制。
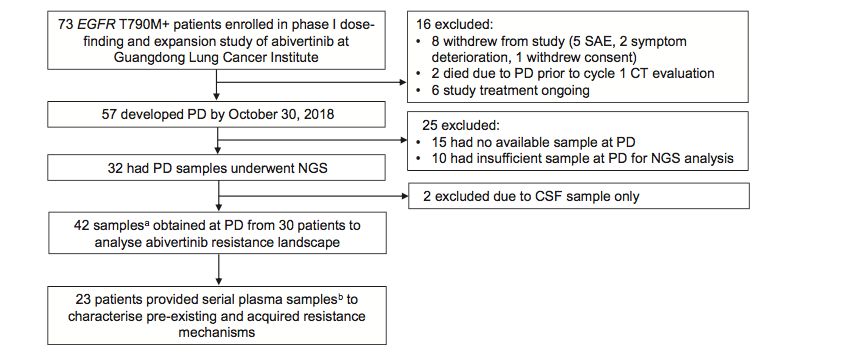
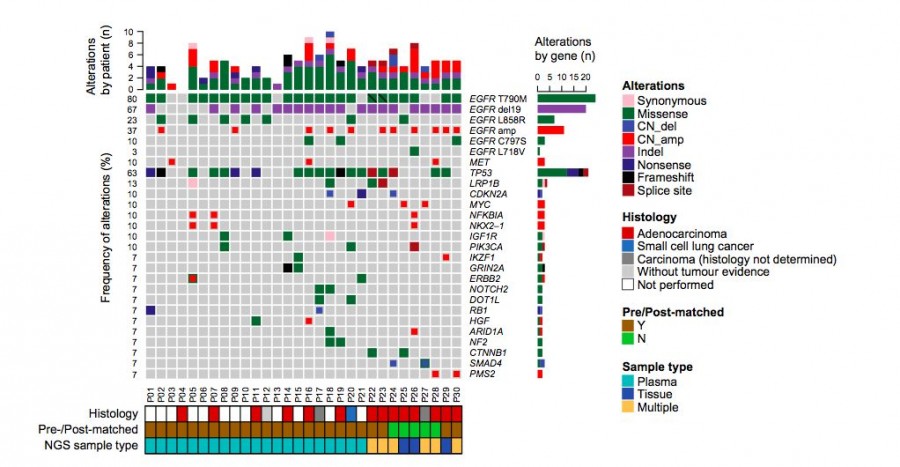
艾维替尼耐药谱的异质性
研究发现:艾维替尼耐药谱呈现异质性,涉及22个(≥2个患者发生)肿瘤相关基因变异,包括EGFR主导耐药机制如EGFR扩增(23%,7/30)、三次突变 (13%,4/30) ;旁路及下游信号通路激活如MET扩增 (10%,3/30)、HER2扩增(3%,1/30)、PIK3CA热点突变(7%, 2/30);以及小细胞转化(7%,1/15)。
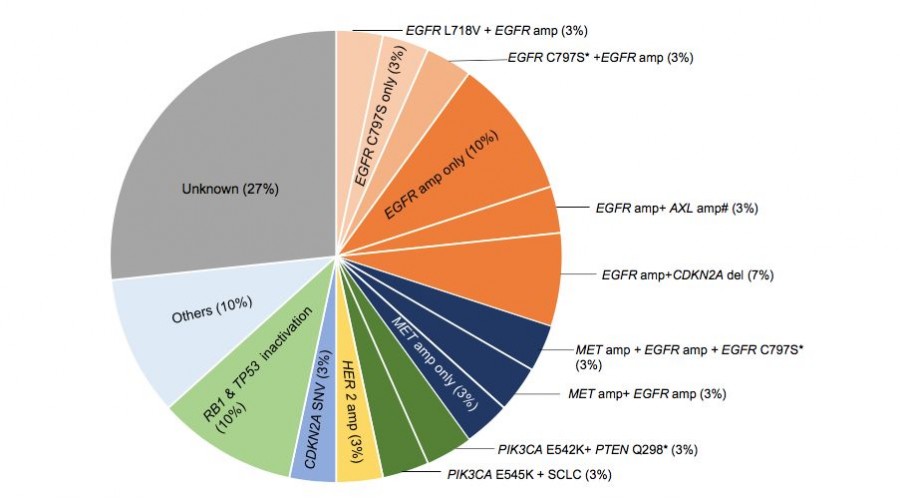
艾维替尼耐药谱的药物特异性
特点一:相对奥希替尼耐药,更少的EGFR T790M突变丢失
在该研究中,27例患者在艾维替尼耐药时检测到EGFR敏感突变,因而可用于评估耐药时EGFR T790M状态。上述患者中15% (4/27)出现EGFR T790M突变丢失,远低于既往研究报道中约42%-68%的奥希替尼耐药患者出现EGFR T790M丢失。
特点二:EGFR扩增可能是艾维替尼的最常见的耐药机制
有趣的是,研究者发现37%(11/30)的艾维替尼耐药患者的耐药样本检测到EGFR扩增。上述患者中的8例接受了艾维替尼治疗基线和耐药标本的配对二代测序,其中4例治疗后获得EGFR扩增,3例艾维替尼治疗基线即存在EGFR扩增,耐药样本检测到EGFR拷贝数上升。因此推定EGFR扩增是上述7例(23%)患者艾维替尼的耐药机制。最后1例提供艾维替尼配对基线/耐药样本的患者,二代测序在治疗基线检测到EGFR扩增,但艾维替尼耐药未检测到EGFR拷贝数上升,同时病理学评估提示小细胞肺癌转化。据此,未推定EGFR扩增是这例患者艾维替尼耐药的机制。其余3例耐药标本中检测到EGFR扩增的患者无艾维替尼基线样本供二代测序,因此无法推断耐药时检测到的EGFR扩增是否主导艾维替尼耐药。
特点三: 首次报道EGFR三次突变介导的艾维替尼耐药,发生率低于既往奥希替尼耐药三次突变的发生率
研究者也首次报道了EGFR三次突变介导的艾维替尼耐药。4例(13%)患者EGFR T790M突变阳性的艾维替尼耐药标本检出EGFR三次突变,包括:EGFR C797S突变(10%, 3/30)和EGFR L718V突变(3%, 1/30)。3例C797S突变均与T790M突变呈顺式。EGFR 三次突变的发生率低于既往研究中21-45%的奥希替尼耐药患者出现EGFR三次突变。
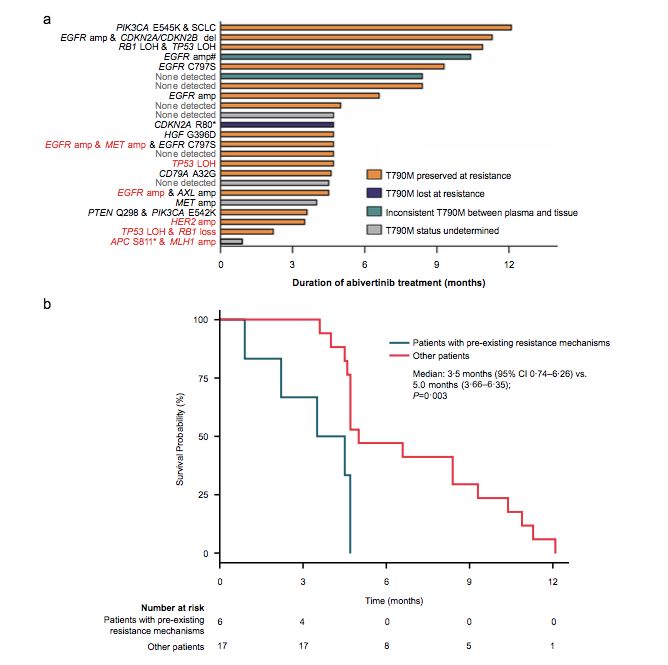
动态血浆监测揭示艾维替尼预存性与获得性耐药机制
研究者进一步对23例接受配对基线/耐药血浆样本二代测序的患者探索了艾维替尼预存性与获得性耐药机制。6例(26%)患者在艾维替尼治疗基线血浆即检出已知耐药机制,包括:并存EGFR和MET扩增、TP53及RB1失活、HER2扩增和EGFR扩增等。
在12例(52%)患者检测到艾维替尼获得性耐药机制,包括:EGFR扩增、EGFR三次突变、MET扩增,PIK3CA热点突变等。此外,上述患者中2例 (9%)既检出了艾维替尼预存性,也检出了获得性耐药机制。根据艾维替尼治疗基线血浆是否检出预存性耐药机制将患者分组,生存分析显示:基线血浆检出预存耐药机制的患者较未检出患者艾维替尼治疗的中位时间显著缩短(中位:3.5个月 vs. 5.0个月,log-rank p =0.003)
研究结论&讨论
1. 在既往EGFR-TKIs治疗失败、晚期EGFR T790M突变阳性的患者中,我国自主研发的第三代EGFR-TKI创新药物艾维替尼与奥希替尼既往报道的耐药基因谱有所不同(一高两低)。
2. EGFR扩增可能是艾维替尼的最常见耐药机制,未来应进一步探索克服EGFR扩增介导艾维替尼耐药的治疗策略。
3. 艾维替尼和奥希替尼耐药基因谱的差异提示:未来应针对不同的第三代EGFR-TKIs分别探索其耐药机制。
4. 由于本研究入组患者来自I期剂量递增/拓展研究,接受艾维替尼治疗剂量不同。因此,本研究揭示的耐药机制有待未来在更大样本量、接受艾维替尼RP2D剂量治疗的患者中进一步验证。
全文链接:https://www.ebiomedicine.com/article/S2352-3964(19)30269-5/fulltext
参考文献:
1. Xu X, Mao L, Xu W, et al. AC0010, an irreversible EGFR inhibitor selectively targeting mutated EGFR and overcoming T790M-induced resistance in animal models and lung cancer patients. Mol Cancer Ther. 2016;15(11):2586-97.
2. Wu YL, Zhou Q, Liu X, et al. Phase I/II study of AC0010, mutant-selective EGFR inhibitor, in non-small cell lung cancer (NSCLC) patients with EGFR T790M mutation. J Thorac Oncol 2017; 12 (1S): S437-38.
3. Lin CC, Shih JY, Yu CJ, et al. Outcomes in patients with non-small-cell lung cancer and acquired Thr790Met mutation treated with osimertinib: a genomic study. Lancet Respir Med. 2018;6(2):107-16.
4. Oxnard GR, Hu Y, Mileham KF, et al. Assessment of resistance mechanisms and clinical implications in patients with EGFR T790M-positive lung cancer and acquired resistance to osimertinib. JAMA Oncol. 2018;4(11):1527-34.
5. Le X, Puri S, Negrao MV, et al. Landscape of EGFR-dependent and -independent resistance mechanisms to osimertinib and continuation therapy beyond progression in EGFR-mutant NSCLC. Clin Cancer Res. 2018;24(24):6195-203.
6. Papadimitrakopoulou VA, Wu YL, Han JY, et al. Analysis of resistance mechanisms to osimertinib in patients with EGFR T790M advanced NSCLC from the AURA3 study. Ann Oncol 2018; 29 (8S): LBA51.
7. Zhou C, Hu M, Zhu X, et al. Resistance Mechanisms of osimertinib in Chinese non-small cell lung cancer patients: Analysis from AURA17 Trial. J Thorac Oncol 2018; 13(10S): S345.


 浙公网安备33080102000126号
浙公网安备33080102000126号